Российские ученые предложили использовать липосомы с магнитными наночастицами в качестве вспомогательного диагностического агента при лечении рака нанопрепаратами. Разработанный исследователями метод может повысить эффективность терапии онкологических заболеваний. Работа была опубликована в журнале Journal of Controlled Release.
Одним из наиболее перспективных и быстроразвивающихся направлений современной фармакологии является адресная (таргетная) доставка лекарственных препаратов. Многие лекарственные препараты обладают серьезными побочными эффектами. Связывание лекарственных препаратов с носителями, которые представляют из себя наночастицы различной природы, позволяет осуществить более прицельную доставку к органу-мишени. Идеальный наноноситель для онкотерапии должен эффективно добираться до раковых клеток, оказывая минимальное воздействие на здоровые ткани организма.
Накопление наночастиц в целевых клетках, а, следовательно, и эффективность терапии, в значительной степени зависит от типа опухоли, проницаемости её сосудов, а также взаимодействия наноносителей с иммунными клетками, в том числе, в микроокружении опухоли. Дополнительная сложность, связанная с использованием нанопрепаратов, заключается в том, что ранее полученная доза лекарства может как повысить, так и ограничить насыщение опухоли препаратом. Исследования показывают, что повторная доза нанопрепарата необязательно ведет себя в организме пациента так же, как первая.
Понимание особенностей взаимодействия различных нанопрепаратов с организмом при мультидозной терапии важно не только для оптимизации существующих протоколов лечения, но и для разработки персонализированных терапевтических решений в будущем. Наносистемы доставки лекарств могут значительно повысить эффективность терапии ряда опухолей за счет так называемого «эффекта улучшенной проницаемости опухолевых сосудов и удержания» (EPR-эффект — enhanced permeability and retention effect), заключающегося в том, что наноструктуры определенного размера (например, липосомы, наночастицы и макромолекулярные препараты) имеют тенденцию к повышенному накоплению в опухолях по сравнению с здоровыми тканями из-за дефектов в стенках опухолевых сосудов. При этом различные опухоли отличаются друг от друга по степени выраженности EPR-эффекта, то есть существует их индивидуальная изменчивость, требующая персонализированного подхода к терапии. Довольно значительная часть злокачественных новообразований не накапливает нанопрепараты в необходимом количестве ввиду пониженной проницаемости опухолевых сосудов и высокого давления в тканях. Это ставит перед учеными задачу разработки эффективной классификации опухолей в зависимости от степени накопления нанопрепаратов, чтобы иметь возможность до начала лечения предсказать его потенциальную эффективность в каждом конкретном случае. Одним из наиболее перспективных решений может стать применение диагностических наноагентов для оценки накопления нанопрепаратов в опухоли. Для дальнейшего развития этой методики критически важно, чтобы введение в организм диагностического агента не оказывало влияния на последующее проникновение лекарственного нанопрепарата и его накопление в опухоли.
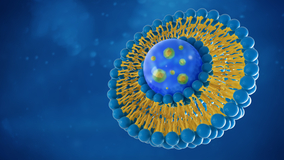
В качестве такого диагностического агента группа ученых из НИТУ «МИСиС», Государственного Научного Центра Социальной и Судебной Психиатрии им. В.П. Сербского, МГУ им. М.В.Ломоносова, Российского национального исследовательского медицинского университета имени Н. И. Пирогова, РХТУ им. Д.И. Менделеева и РАН предложила использовать магнитные липосомы — липидные пузырьки, содержащие магнитные наночастицы из окскида железа. Выбор объясняется, в частности, тем, что большинство клинически одобренных нанопрепаратов, применяющихся при терапии опухолей, являются липосомами, наполенными тем или иным лекарственным средством (в данном исследовании применяли липосомальный доксорубицин — Доксил или Келикс). Магнитные липосомы призваны смоделировать липосомальную формуляцию лекарственного препарата — они совпадали с ней по размерам (около 100 нм в диаметре) и липидному составу, а за счет магнитных наночастиц за накоплением магнитных липосомам в опухолях можно было наблюдать с помощью магнитно-резонансной томографии (МРТ).
В ходе исследования ученые также с помощью интравитальной конфокальной флуоресцентной микроскопии наблюдали за биораспределением аналогичных липосом с флуоресцентной меткой в организме после введения первой и повторной доз нанопрепарата. Наблюдения показали, что ранее полученная пациентом диагностическая доза липосомного нанопрепарата не оказывает влияние на поведение последующей дозы липосом.
Что наиболее важно, использование магнитных липосом позволяет проводить неинвазивный отбор опухолей с хорошим накоплением липосом, т.е. потенциально поддающихся лечению липосомными препаратами. Таким образом, при использовании в качестве вспомогательного диагностического агента магнитные липосомы могут стать ценным инструментом оценки эффективности терапии нанопрепаратами при выборе персонализированного подхода к терапии опухолей.
«В терапевтическом эксперименте на мышах до начала лечения животных снимали на МРТ, далее внутривенно вводили диагностические магнитные липосомы и через 6 часво оценивали их накопление в опухолях, сравнивая, как выглядит опухоль на МРТ до и после инъекций. Были выделены группы с опухолей с эффективным и неэффективным накоплением магнитных липосом. Далее все животные получали одинаковое лечение липосомальным доксорубицином. Опухоли с эффективным накоплением магнитных липосом отвечали на лечение лучше, чем опухоли со слабо выраженным накоплением диагностического агента. В аналогичном эксперименте с применением для терапии традиционной формуляции доксорубицина (без липосомной упаковки), различий ответа опухолей в выделенных группах по эффективности накопления магнитных липосом отмечено не было, т.е. методика сработала для предсказания эффективности именно липосомальными онкопрепаратами», — поясняет основной автор исследования, кандидат биологических наук, инженер
1-й категории лаборатории «Биомедицинские наноматериалы» НИТУ «МИСиС», младший научный сотрудник биологического факультета МГУ имени М. В. Ломоносова Степан Водопьянов.